1月19日�����,南京大學(xué)任昊楨研究團(tuán)隊(duì)在期刊《Cell Death Discovery》上發(fā)表了題為“CHEK2 knockout is a therapeutic target for TP53-mutated hepatocellular carcinoma”的研究論文��,本研究發(fā)現(xiàn)了一種新的藥物靶點(diǎn)���,通過(guò)線粒體ATP作用于TP53突變型HCC細(xì)胞���,成功克服了Nultin-3單獨(dú)治療無(wú)法誘導(dǎo)腫瘤細(xì)胞死亡的局限性。
研究背景
肝細(xì)胞癌(HCC)是常見(jiàn)的肝癌類(lèi)型�,是全球癌癥相關(guān)死亡的第五大原因����。隨著肝癌發(fā)病率的不斷上升,現(xiàn)有的藥物治療效果有限�,迫切需要?jiǎng)?chuàng)新的治療策略。雖然索拉非尼和侖伐替尼等藥物在改善患者預(yù)后方面取得了一些成功��,但多中心研究顯示���,由于耐藥和副作用�,它們對(duì)長(zhǎng)期生存的影響有限。因此�,積極尋找新的有效藥物靶點(diǎn)以改善HCC患者的預(yù)后具有重要的臨床意義。
研究進(jìn)展
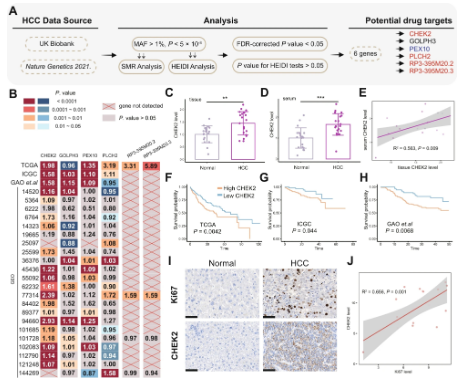
為了確定潛在的HCC藥物靶點(diǎn)���,研究人員首先搜索了兩個(gè)HCC GWAS數(shù)據(jù)集(ICD10 C22.0, ieu-b-4953)作為結(jié)果數(shù)據(jù)����,并從eQTLgen數(shù)據(jù)庫(kù)下載數(shù)據(jù)作為參考數(shù)據(jù)�。通過(guò)SMR分析,研究人員根據(jù)每個(gè)數(shù)據(jù)集中的頂部snp分別鑒定出726個(gè)和314個(gè)潛在的藥物靶基因��。接下來(lái)��,研究人員研究了這些潛在靶基因在HCC組和正常組中的表達(dá)水平��。根據(jù)觀察�����,研究人員假設(shè)CHEK2可能在HCC中發(fā)揮更重要的作用��。因此�����,研究人員選擇在后續(xù)研究中進(jìn)一步研究CHEK2。為此��,研究人員觀察了血清樣本和組織樣本�����。此外�����,為了研究CHEK2在HCC中的臨床指標(biāo)���,研究人員選擇了TCGA�、ICGC和GAO等隊(duì)列����,研究人員發(fā)現(xiàn)CHEK2高的組比CHEK2低的組預(yù)測(cè)更低的總生存率�����。另外�����,與低CHEK2組相比,研究人員發(fā)現(xiàn)高CHEK2組具有更差的無(wú)病間期(DFI)����,疾病特異性生存(DSS)和無(wú)進(jìn)展間期(PFI)。然后����,通過(guò)免疫組化分析,研究人員發(fā)現(xiàn)HCC組的CHEK2蛋白水平明顯高于正常組��。另外����,在HCC樣本中,CHEK2和Ki67的IHC水平之間存在很強(qiáng)的相關(guān)性�。
圖1:CHEK2可能是HCC的潛在藥物靶點(diǎn)
為了進(jìn)一步研究CHEK2和TP53突變的HCC細(xì)胞之間的關(guān)系,研究人員分析了三個(gè)隊(duì)列(TCGA���、ICGC和GAO等)的數(shù)據(jù)����,發(fā)現(xiàn)CHEK2表達(dá)在有TP53突變的組織中顯著上調(diào)�����。此外,研究人員還比較了CHEK2低水平組和高水平組的基因組���。分析顯示��,高CHEK2組的TP53突變頻率較高�。研究人員進(jìn)行了克隆形成�、Edu實(shí)驗(yàn)、β-半乳糖苷酶染色和細(xì)胞周期實(shí)驗(yàn)�����。研究人員觀察到����,加入Nultin-3可以更明顯地誘導(dǎo)肝癌細(xì)胞停滯在G0/G1期,抑制增殖���,進(jìn)一步促進(jìn)衰老����。
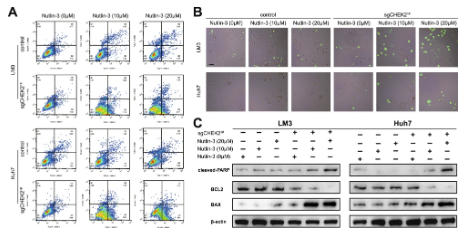
研究表明����,nutlin -3介導(dǎo)的p53激活可以誘導(dǎo)可逆的腫瘤細(xì)胞周期阻滯,而不會(huì)引起細(xì)胞凋亡��。研究人員發(fā)現(xiàn)在HCC細(xì)胞系中敲除CHEK2會(huì)導(dǎo)致細(xì)胞凋亡增加��,尤其是在細(xì)胞凋亡的早期階段�。此外,研究人員通過(guò)評(píng)估caspase-3綠色凋亡檢測(cè)試劑驗(yàn)證了上述結(jié)果�����。研究人員發(fā)現(xiàn)CHEK2敲除后HCC細(xì)胞凋亡增加��。此外����,免疫印跡結(jié)果證實(shí)了這些發(fā)現(xiàn)。因此��,敲除CHEK2可觸發(fā)Nultin-3處理的HCC細(xì)胞凋亡����。
圖2:敲除CHEK2可觸發(fā)nultin -3處理的HCC細(xì)胞凋亡
研究結(jié)論
在本研究中,研究人員通過(guò)MR篩選初步確定了CHEK2作為HCC的藥物靶點(diǎn)��,并發(fā)現(xiàn)CHEK2敲除選擇性地誘導(dǎo)TP53突變細(xì)胞的生長(zhǎng)停滯。此外��,研究人員觀察到Nultin-3和CHEK2敲除的聯(lián)合更有可能通過(guò)線粒體ATP途徑抑制HCC�����??傊狙芯繛門(mén)P53突變的HCC細(xì)胞引入了一個(gè)假定的靶點(diǎn)���,并克服了Nultin-3單獨(dú)不能誘導(dǎo)腫瘤細(xì)胞死亡的局限性���。
聲明:本文版權(quán)歸原作者所有,轉(zhuǎn)載文章僅為傳播更多信息�����,如作者信息標(biāo)記有誤�����,或侵犯您的版權(quán)���,請(qǐng)聯(lián)系我們�����,我們將在及時(shí)修改或刪除內(nèi)容��,聯(lián)系郵箱:marketing@360worldcare.com